

500.000 Menschen erkranken allein in Deutschland jedes Jahr neu an Krebs. Experten erwarten, dass diese Zahl bis 2030 um fast 20 Prozent steigen wird. Derzeit sind die häufigsten Krebserkrankungen bei Männern Prostatakrebs, Lungen- und Darmkrebs, bei Frauen sind es Brustkrebs, Darm- und Lungenkrebs. Neben den bekannten Behandlungsoptionen wie Operation, Chemo- und Strahlentherapie gibt es mittlerweile auch hoch entwickelte neue Methoden. Einer der innovativen Ansätze ist die sogenannte CAR-T-Zelltherapie, die unter anderem im Helios Klinikum Berlin-Buch eingesetzt wird.
(Veröffentlicht: Februar 2024)
Fresenius-Redakteurin Brigitte Baas spricht mit Prof. Bertram Glaß, Chefarzt für Hämatologie und Zelltherapie im Helios Klinikum Berlin-Buch, über die Chancen und Risiken dieser Behandlung.
Herr Prof. Dr. Glaß, bitte erklären Sie kurz, was das Wirkprinzip der CAR-T-Zelltherapie ist und wie diese Therapie funktioniert.
Prof. Dr. Bertram Glaß: Die CAR-T-Zelltherapie ist eine Form der Immuntherapie, die Abwehrzellen des Patienten verwendet, um zielgerichtet bösartige Zellen im Patienten zu zerstören und – anders als z. B. die klassische Chemotherapie – gesunde Gewebe und Organe möglichst unbeeinträchtigt zu lassen. Für die Therapie entnehmen wir dem Patienten zunächst körpereigene T-Zellen, die eine Schlüsselrolle in der Immunabwehr spielen, und verändern diese genetisch. Dadurch erwerben diese T-Zellen die Fähigkeit, Krebszellen zu erkennen. Diese Zellen werden dem Patienten anschließend wieder per Infusion verabreicht – mit dem Ziel, im Körper Prozesse anzustoßen, die Krebszellen zerstören. Bislang steht diese Therapie für die Behandlung von speziellen Tumoren des menschlichen Abwehrsystems zur Verfügung. Die Ausweitung auf die Behandlung anderer häufig vorkommender Tumoren ist Gegenstand laufender wissenschaftlicher Untersuchungen. (Mehr Infos dazu weiter unten.)
Jede CAR-T-Therapie wird also für eine bestimmte Person mit einer bestimmten Erkrankung produziert. Ist das die Personalisierung, von der derzeit immer wieder die Rede ist? Und was genau sind aus Patientensicht die Vorteile einer solchen Behandlungsweise?
Prof. Glaß: Die CAR-T-Therapie ist sicher ein erster Schritt und eine mögliche Basis für eine zukünftige echte personalisierte Medizin.
Es gibt parallel hierzu weitere Ansätze wie etwa andere Formen der Immuntherapie oder die Ermittlung von krebsspezifischen genetischen Veränderungen in der Krebszelle, die von speziellen Medikamenten angegangen werden. Alle diese Ansätze werden in der personalisierten Tumormedizin kombiniert und ermöglichen eine sehr gezielte Behandlung für genau die Erkrankung eines speziellen Patienten. Im Vergleich zu einer One-size-fits-all-Herangehensweise kann dies zu einer effektiveren Tumorabwehr führen und gleichzeitig zu wirksamen Therapien mit reduzierten Nebenwirkungen. Eine Personalisierung ermöglicht es zudem, die Behandlung an den Verlauf der Krankheit anzupassen, was sie insgesamt präziser und effizienter macht als alles, was wir bislang in der Krebsmedizin hatten.
Für welche Arten von Krebserkrankungen ist denn die CAR-T-Zelltherapie ein vielversprechender Ansatz?
Prof. Glaß: Im Moment sind in Deutschland und anderen europäischen Ländern zwei Gruppen von Erkrankungen für die CAR-T-Therapie zugelassen. Sie kann aktuell bei bestimmten bösartigen Erkrankungen des Immunsystems und der Blutbildung eingesetzt werden – etwa bei der akuten lymphatischen Leukämie (ALL) und einigen Non-Hodgkin-Lymphomen (NHL) sowie dem Multiplen Myelom. Diese gelten vor allem bei einem Rückfall nach ersten Therapien als schwer behandelbar. Für sie gibt es mit der CAR-T-Zelltherapie eine Ansprechrate von bis zu 80 Prozent – und für bis zu 40 bis 50 Prozent langanhaltende Rückbildungen, d. h. möglicherweise Heilungen. Das heißt, vier Fünftel aller Patientinnen und Patienten kann mit der Behandlung geholfen werden!
Wie bei jeder Therapie gibt es sicher auch bei der CAR-T-Zelltherapie Nebenwirkungen. Welche sind das?
Prof. Glaß: Das CAR-T-Zell-Verfahren beeinflusst neben den Krebszellen auch gesunde Immunzellen. Das Verfahren ist sehr effektiv und kann durch die heftige Entzündungsreaktion und möglicherweise auch durch Wirkung auf einige unbeteiligte gesunde Zellen im Nervensystem Nebenwirkungen hervorrufen. Nach der Infusion der CAR-T-Zellen kann es daher zu unterschiedlichen Symptomen kommen, etwa zu Fieber, Schüttelfrost, niedrigem Sauerstoffgehalt im Blut, schnellem Herzschlag oder geringem Blutdruck. Außerdem sind Störungen des Nervensystems, ein Mangel an Antikörpern und Infektionen möglich. Die gute Nachricht: All diese potenziellen Nebenwirkungen beobachten wir genau, alle können wir gut behandeln – und sie gehen vorüber. In der Summe ist das Verhältnis zwischen Wirkung und Nebenwirkung erheblich günstiger als bei älteren Verfahren wie der Hochdosis-Chemotherapie, die durch CAR-T-Therapie daher immer weiter ersetzt werden.
Die CAR-T-Therapie ist sicher ein erster Schritt und eine mögliche Basis für eine zukünftige echte personalisierte Medizin.
Am 4. Februar ist Weltkrebstag. Er trägt das Motto „Versorgungslücken schließen“. Diese Lücke in der Versorgung bezieht sich auf die Zugangsmöglichkeiten, die Krebspatienten hinsichtlich Diagnose und Behandlung haben. Wie kann denn die CAR-T Zelltherapie dazu beitragen, diese bestehende Lücke zu schließen?
Prof. Glaß: Die Zugangsmöglichkeiten sind – zugegeben – auf der Welt sehr unterschiedlich. Wir sind hierzulande, das muss man sagen, diagnostisch und therapeutisch sehr gut aufgestellt. Versorgungslücken in unserem Land bestehen, was die Therapie angeht, immer dort, wo unsere wissenschaftlichen Erkenntnisse für die Etablierung einer wirksamen und wenn möglich heilenden Therapie noch nicht ausreichen. Bei Leukämien, Lymphomen sowie dem sogenannten Multiplen Myelom ist es nun gelungen, diese Lücke zu verkleinern. Die CAR-T-Zelltherapie ist aber auch ein wichtiger Hoffnungsträger, wenn es um die Schließung der Lücken bei den anderen, heute noch nicht heilend zu behandelnden Krebsarten geht. Aktuell kann aber nur ein sehr kleiner Teil aller Patientinnen und Patienten von dieser innovativen Behandlungsform profitieren, und dies auch nur in entwickelten Ländern wie dem unseren. Denn sie ist sehr aufwendig und damit teuer und wird bislang nur eingesetzt, wenn andere Therapieoptionen versagt haben.

Woran genau liegt das? Und wie könnte die CAR-T-Zelltherapie für mehr Patientinnen und Patienten und auch für andere Krebsarten verfügbar gemacht werden?
Prof. Glaß: Die Therapieform ist deshalb teuer und aufwendig, weil der Herstellungsprozess der CAR-T-Zellen lange dauert und für jeden Patienten einzeln durchlaufen werden muss. Derzeit beträgt er rund 14–28 Tage. Wir gehen hier mit lebenden Zellen um, die in sehr aufwendigen Fabriken unter strengsten kontrollierten Bedingungen bearbeitet werden. Auch die Lieferkette ist sehr komplex und benötigt gewisse Strukturen. So muss im Krankenhaus etwa ein eigenes hoch qualifiziertes Hämatologie-Zentrum vorhanden sein. Diese Voraussetzungen erfüllen nicht einmal alle Krankenhäuser der Maximalversorgung. Es gibt aber mittlerweile viele Bestrebungen in der Branche, die Herstellung zu verkürzen und das Verfahren günstiger zu machen.
Wir haben bislang viel darüber gesprochen, wie Krebserkrankungen behandelt werden können. Helios weist ganz aktuell aber auch auf die Bedeutung der Krebsvorsorge hin: also Prävention und Früherkennung. Welchen Stellenwert messen Sie als Behandler der Prophylaxe zu?
Prof. Glaß: Wir alle wissen ja: Je früher eine Krebserkrankung erkannt wird, desto einfacher und erfolgversprechender ist in der Regel ihre Behandlung und desto höher sind auch die Überlebenschancen. Die Krebsfrüherkennung birgt im Kontext hier das vielleicht größte Potenzial für die Therapie! Die Check-ups beim Arzt mit Blut- und Urinuntersuchungen sind eine wichtige Säule, außerdem Mammografie, Darmspiegelung und Hautkrebs-Screening. Ziel ist es stets, den Krebs und seine Vorstufen möglichst früh zu entdecken.
Was ist noch wichtig bei der Prophylaxe?
Prof. Glaß: Wenn sie wirksam sein soll, müssen wir auch die Primärprävention erwähnen. Sie zielt darauf ab, die Entstehung von Krebs von vornherein zu verhindern. Damit sind Maßnahmen wie eine gesunde, ausgewogene Ernährung, Verzicht auf Alkohol und Nikotin oder Schutz vor UV-Licht und anderes mehr gemeint. Primärprävention ist also letztlich das, was jede und jeder von uns selbst am meisten beeinflussen kann. Das Erstaunliche daran: Primärprävention und Früherkennung zusammengenommen könnten die Krebssterblichkeit um bis zu 75 Prozent senken.
Experten stellen aber immer wieder fest, dass viele Menschen dieses Potenzial gar nicht nutzen. Wie erklären Sie sich das?
Prof. Glaß: Tja, das ist wohl in der Psychologie des Menschen begründet. Solange kein Schaden da ist, ist die Gefahr zu abstrakt. Und es gibt immer Beispiele von Menschen, bei denen alles gut geht – sie werden kettenrauchend 90 Jahre alt. Diese seltenen Beispiele müssen dann herhalten, wenn viel getrunken, zu süß und zu fett gegessen und sich zu wenig bewegt wird. Bei vielen spielt sicher auch ein gewisser Fatalismus mit rein: Da bestimmte Krebsarten überwiegend zufällig entstehen, etwa Lymphome, Hirntumoren und auch Krebserkrankungen bei Kindern, kann man ihnen nach heutigem Wissen kaum durch einen gesunden Lebensstil vorbeugen. Aber klar, einen Patienten hier in der Klinik zu behandeln und ihm im wahrsten Sinne des Wortes das Leben zu retten – und ihn dann vor der Tür rauchen zu sehen, das ist der wirklich harte Teil unseres Berufes. Aber auch das hält mich nicht davon ab, zu hoffen, dass wir für alle Krebsarten eines Tages effektive Therapieformen finden werden. Es passiert so viel Innovation gerade – und wir sind ein Teil davon!
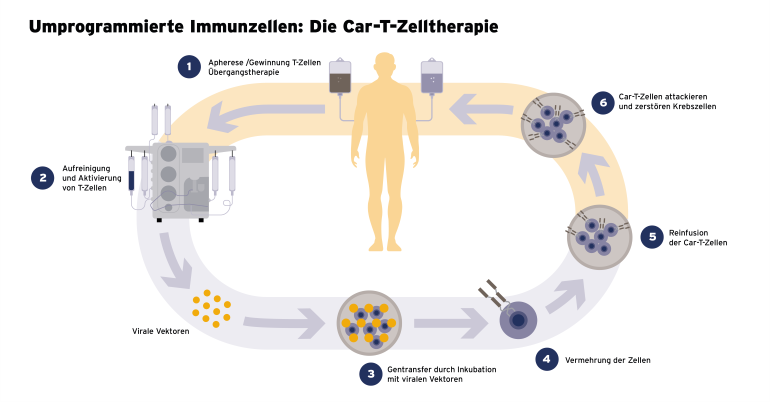
ⓘ Die Car-T-Zelltherapie
Bei der CAR-T-Zell-Therapie werden die T-Zellen des Körpers, die Teil des Abwehr- bzw. Immunsystems sind, mit so genannten CARs angereichert. CAR steht für chimärer Antigenrezeptor. Die entnommenen T-Zellen werden im Labor genetisch modifiziert. Durch diese genetische Veränderung erwerben die T-Zellen die Fähigkeit, Krebszellen zu erkennen, welche ein spezifisches Ziel-Antigen auf ihrer Oberfläche tragen. Dieses Ziel-Antigen ist oft charakteristisch für bestimmte Krebsarten. Aus den T-Zellen sind damit CAR-T-Zellen geworden.
Diese werden anschließend den Patienten wieder per Infusion zugeführt und zirkulieren dann im Blutkreislauf. Wenn sie nun auf Krebszellen mit dem spezifischen Ziel-Antigen treffen, bindet der extrazelluläre Bereich des CARs gezielt an dieses Antigen auf der Oberfläche der Krebszelle und aktiviert die CAR-T-Zelle. Dies führt zu einer rapiden Vermehrung der T-Zellen und zur Freisetzung von zytotoxischen Molekülen, die die Krebszelle zerstören.
Ein entscheidender Aspekt der CAR-T-Zelltherapie ist die Fähigkeit der modifizierten T-Zellen, im Körper des Patienten eine langfristige Immunantwort aufrechtzuerhalten. Dies kann dazu beitragen, wiederholte Angriffe auf Krebszellen über einen längeren Zeitraum aufrechtzuerhalten. Die genaue Funktionsweise kann je nach den spezifischen Protokollen und Ziel-Antigenen, die in der Therapie verwendet werden, variieren.
Contact
Helios Klinikum Berlin-Buch
Schwanebecker Chaussee 50
13125 Berlin
T +49 (0)30 94 01-0

